3 Technique d'extraction
| A - Exemple :Extraction d'une huile essentielle naturelle : le LIMONČNE |
- MACÉRATION
:Le limončne est présent dans l'écorce d'orange ou de citron. Il
faut commencer par faire macérer les écorces d'orange dans l'eau
chaude et de les mixer pour faire éclater les cellules végétales pour
libérer les composés organiques.
- DISTILLATION : Il faut ensuite isoler le limončne de la solution et des débris végétaux. Pour cela on peut procéder ŕ une HYDRODISTILLATION . La phase gazeuse qui se dégage par chauffage contient de l'eau et des produits organiques dont le limončne. La condensation de la vapeur entraîne sa séparation en 2 phases liquides ( aqueuse et organique)
Compléter la légende du montage d'hydrodistillation
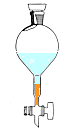
- RELARGAGE et DÉCANTATION : On verse ensuite la totalité du distillat dans une AMPOULE ŕ DÉCANTER en ajoutant du chlorure de sodium pour diminuer la solubilité (déjŕ trčs faible) du limončne dans l'eau. Le relargage consiste ŕ rendre moins soluble dans l'eau des composés organiques en y dissolvant des composés ioniques.
La densité du limončne étant d=0.84 va t-on observer la situation 1 ( limončne au-dessus de la phase aqueuse) ou la situation 2 (limončne en dessous)?
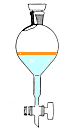
- SECHAGE : L'extrait organique récupéré ainsi est ensuite séché (élimination des derničres traces d'eau) par du sulfate de magnésium anhydre puis filtré et récupéré dans un tube ŕ essai.
-
ANALYSE : Il ne reste plus qu'ŕ comparer l'extrait obtenu avec du limončne commercial (pur ŕ 98%). Pour cela il suffit de faire une CHROMATOGRAPHIE.
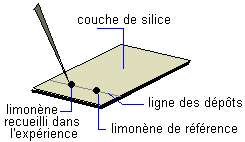 |
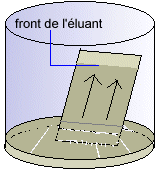
Une goutte du limončne de référence et une
goutte du limončne recueilli sont déposées au męme niveau sur une ligne que l'on
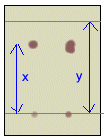
appellera la ligne des dépôts. La plaque de silice (SiO2) est ensuite déposée dans un récipient contenant un éluant(par exemple le cyclohexane C6H12), la ligne des dépôts au-dessus de la surface de l'éluant. La phase fixe (l'adsorbant SiO2) et la phase mobile (l'éluant C6H12) présentent des polarités différentes. En fonction de ces polarités les matičres organiques déposées auront tendance ŕ migrer avec l'éluant ou ŕ se fixer sur la plaque. Elles vont donc progresser ŕ la surface ŕ des vitesses différentes de l'éluant. On retire la plaque avant que l'éluant n'arrive en haut de la plaque . On repčre le front de l'éluant puis on sčche la plaque. Les taches n'apparaissent pas. Il faut les révéler en plongeant la plaque dans une solution oxydante de permanganate. Il apparaît alors des taches brunes. Si les 2 taches se trouvent ŕ la męme hauteur le produit testé est bien du limončne. On peut aussi déterminer le rapport frontal du composé : Rf Rf = rapport des distances parcourues par le solvant et le composé = x/y |
|
|
|
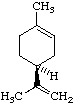
LA MOLECULE DE LIMONENE
|
La molécule de limončne comporte un carbone asymétrique ( le carbone n°5) . Il existe donc 2 énantiomčres non superposables:
|
||
|
|
|