ATOMES |
:ELECTRONS : |
|||
Calcul de la masse de l'atome d'HELIUM:
La masse des électrons peut donc bien être considérée comme négligeable devant celle du noyau.
La masse volumique du noyau d'hélium est de l'ordre de 232 millions de tonnes par cm3 ! Ce serait la masse volumique de la matière habituelle si les noyaux d'atomes étaient jointifs entre eux sans nuages d'électrons. On peut donc dire que la matière habituelle est essentiellement constitué de vide.


conclusion
NOYAU : protons (+) et neutrons(0)
NUAGE ELECTRONIQUE : électrons (-)
Un atome est électriquement neutre:
nombre de p(+) = nombre d'électrons( -)
La masse d'un atome est concentrée dans son noyau:
m(proton) » m(neutron). >>
m(electron).
Donc m(atome) = nombre de nucléon X m(proton)
La matière a une structure lacunaire car elle est essentiellement constituée de vide
Graphe du rayon atomique en fonction du nombre de proton d'un noyau
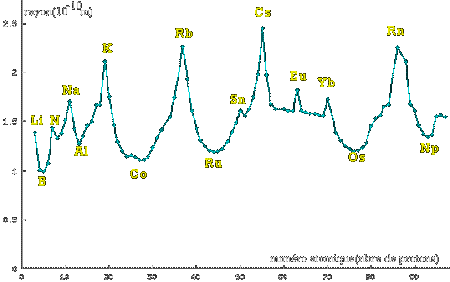
Sur ce graphe sont représentés les rayons d'une centaine d'atomes. On remarque que le rayon d'un atome (donc son volume) ne dépend pas du nombre d'électrons autour du noyau. La valeur moyenne se situe autour de 0.15 nm.
Règles de répartition:
Les électrons se répartisent en couches d'énergie. Chaque couches est caractérisée par un nombre entier n. Ces couches se nomment K, L, M, N, ....
1- Principe de PAULI:
Chaque couche ne peut contenir au maximum que 2n² électrons
| nombre n | 1 |
2 |
3 |
4 |
| couche | K |
L |
M |
N |
| nbre maxi d'e : 2n² | 2 |
8 |
18 |
32 |
2- principe de construction:
Dans l' état le plus stable des atomes, les électrons occupent
successivement les niveaux en commençant par les numéro les
plus faibles. La dernière couche occupée (couche externe) a
une grande importance au niveau chimque.
EXEMPLE :
La plupart des atomes ont tendance à perdre ou à gagner des électrons pour former des ions monoatomiques. Seuls les gaz rares ne forment pas d'ions:
| hélium | He (Z=2) | K2 |
| néon | Ne (Z=10) | K2L8 |
| Argon | Ar (Z=18 | K2L8M8 |
| Krypton | Kr (Z=36) | K2L8M18N8 |
Ils ont tous 8 électrons sur la couche externe (sauf He car la couche K ne peut en contenir plus de 2). Tous les autres atomes auront tendance à perdre ou à gagner des électrons pour avoir une couche externe à 8 électrons. C'est la règle de l'octet. ( dans le cas de la couche K ce sera 2 électrons et l'on parle de règle du duet)
ions positifs(cations) |
||
| SODIUM Na (Z=11) K2L8M1 | perd 1 e | ion sodium Na+ K2L8 |
| Beryllium Be (Z=4) K2L2 | perd 2 e | ion béryllium Be2+ K2 |
ions négatifs (anions) |
||
| Soufre S (Z=16) K2L8M6 | gagne 2 e | ion sulfure S2- K2L8M8 |
| Fluor F (Z=9) K2L7 | gagne 1e | ion fluorure F- K2L8 |